上海净信实业发展有限公司品牌商
12 年
手机商铺
- NaN
- 0.20000000000000018
- 1.2000000000000002
- 0.20000000000000018
- 3.2
推荐产品
公司新闻/正文
应用案例 | 净信JX-ZLN-BN真空离心浓缩仪在蛋白质纯化后处理中的应用
86 人阅读发布时间:2026-04-29 17:32
1. 背景:为什么纯化后处理如此关键?
跑完柱子,拿到一管洗脱液——然后呢?浓度够不够?缓冲体系能不能直接上机?放一晚上活性还剩多少?这些问题不解决,纯化做得再干净,下游实验照样翻车。后处理看着像收尾,实际上是决定样品"能不能用"的最后一道关卡。
1.1 纯化后样品面临的典型问题
(1)体积偏大,浓度不足
蛋白质从层析柱上下来时,常常存在体积偏大、浓度不足的问题。洗脱峰展宽导致目标蛋白分散在较大的收集体积中,终浓度往往偏低。对于酶动力学测定、结晶筛选、质谱分析等下游实验而言,这样的浓度远远不够。
(2)缓冲体系含有干扰组分
不同类型的层析使用不同的缓冲液体系。体系里还带着盐、咪唑、甘油或其他添加剂,这些组分如果不去除或稀释,可能直接干扰下游检测结果的准确性。
(3)目标蛋白对环境条件敏感
蛋白质作为生物大分子,其三维构象和生物学活性对外界条件高度敏感。目标蛋白本身活性脆弱,对温度、pH和剪切力都比较敏感。如果直接上机检测或冻存,结果往往不稳定。
1.2 后处理的实质
后处理的意义并不只是"把样品收小一点",更重要的是把样品调整到适合下游使用的状态。比如用于Western blot、酶动力学测定、质谱分析或晶体筛选,不同场景对蛋白的浓度、缓冲体系和完整性要求都不一样。
可以说,后处理做得稳,前面的纯化才算没有白费。

2. 实验室蛋白纯化后处理的四大痛点
在实际操作中,蛋白纯化后处理环节最常遇到以下四个问题:
|
痛点 |
具体表现 |
对实验的影响 |
|
蛋白变性 |
温度过高或停留时间过长,容易导致构象变化和活性下降 |
下游功能实验结果失真 |
|
回收率不稳 |
操作步骤多、人工判断多,样品损失往往发生在细节里 |
珍贵样品浪费,实验成本增加 |
|
缓冲体系不匹配 |
盐分和添加剂残留,会直接影响后续检测结果的准确性 |
酶活、质谱、ELISA等结果干扰 |
|
批次一致性差 |
方法不固定、参数靠经验,容易造成实验重复性不足 |
多批次数据不可比,论文和项目数据可信度下降 |
这些问题看似是"操作细节",但实际上决定了前面整个纯化流程是否白费。
3. 三种主流浓缩技术的原理与选择
目前实验室常用的蛋白浓缩技术主要包括以下三类:
3.1 超滤浓缩
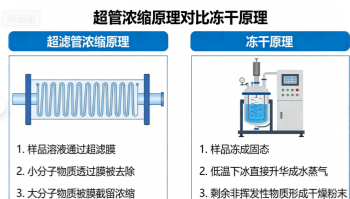
● 原理:利用具有特定分子量截留值(MWCO)的半透膜,在离心力驱动下让溶剂和小分子通过膜孔,而目标蛋白被截留在膜上方,从而实现浓缩。
● 优势:操作直观,实验室最常见的方法之一。同时具有一定的缓冲液置换功能(反复加液离心)。
● 局限:疏水性蛋白容易吸附在膜面上,造成回收率下降;离心过程中的剪切力对部分蛋白可能造成机械损伤;浓缩终点依赖操作者人工判断,批次间一致性受限于个人经验。
3.2 冷冻干燥
● 原理:将蛋白溶液在超低温下冻结成固态,随后在真空条件下使冰直接升华为水蒸气,最终获得蛋白干粉。
● 优势:更适合长期保存和运输,可把蛋白制成干粉,体积极小,便于储存和邮寄。
● 局限:周期较长,通常需要12~48小时甚至更久;冻结和升华过程中,冰晶形成和界面效应可能对蛋白构象造成损伤;对部分活性蛋白需要谨慎评估。
3.3 真空离心浓缩
● 原理:在密封腔体内同时施加离心力和真空,降低溶剂沸点,使溶剂在低温下即可高效蒸发;离心力将液面压向管底,防止液体暴沸和飞溅;配合主动控温系统,可将样品温度精确控制在保护范围内。
● 优势:处理效率高;全程低温运行,蛋白不接触高温,活性保护效果好;无膜接触,避免吸附损失;参数可程序化设置,批次一致性高;可多管并行处理,适合多批次高通量需求。
● 局限:需配备专用仪器;对于需同时完成缓冲液置换的场景,需配合透析或脱盐柱使用。
3.4 选型建议
|
应用需求 |
推荐方法 |
理由 |
|
常规重组蛋白浓缩 |
超滤浓缩 |
操作简单,设备普及率高 |
|
样品需长期保存/运输 |
冷冻干燥 |
干粉形态稳定性好 |
|
温度敏感型蛋白/多批次并行 |
真空离心浓缩 |
低温保护活性,参数可控,批次一致性高 |
|
小体积、高通量场景 |
真空离心浓缩 |
多管同时处理,效率高 |
|
浓缩同时需缓冲液置换 |
超滤浓缩(反复稀释-浓缩) |
超滤膜同时截留蛋白、透过小分子 |
4. 真空离心浓缩技术详述
4.1 三重协同机制深入解析
真空离心浓缩仪的核心在于三重物理机制的协同配合:
|
机制 |
作用 |
对蛋白样品的意义 |
|
真空系统 |
降低腔体内气压,使溶剂(水)沸点显著下降 |
溶剂可在远低于37℃的条件下蒸发,从源头避免热变性 |
|
离心力场 |
将液体压向管底 |
抑制暴沸和飞溅,防止样品损失和交叉污染 |
|
主动控温 |
精确控制腔体与样品温度 |
确保蛋白全程处于设定温度,构象和活性得到有效保护 |
这三个机制任何一个单独使用都不够——只抽真空会暴沸,只离心不能降低沸点,只控温不能加速蒸发。正是三者的联合,才使得"低温条件下的高效溶剂去除"成为可能。
4.2 仪器方案:净信JX-ZLN-BN真空离心浓缩仪(升级冷冻款)

核心设计理念解读:
(1)-10℃至100℃宽幅控温
这是该仪器区别于普通真空离心浓缩仪的关键参数。-10℃至4℃的低温区间为热敏性蛋白(如酶、抗体、不稳定的重组蛋白)提供了安全的操作温度窗口——蛋白在整个浓缩过程中始终处于冷链保护状态,避免因温度波动而导致的构象变化。而100℃的上限则兼容了有机溶剂样品(如乙腈、甲醇水溶液等)的蒸发需求,使仪器的应用范围不局限于蛋白领域,一台设备可覆盖生命科学、化学分析、环境检测等多个方向。
(2)离心、真空、控温三位一体
不是简单的"抽真空+加热",而是三个物理手段相互补位:真空提供蒸发驱动力,离心保障过程安全,控温守住样品活性底线。这种设计理念决定了它对生物样品的友好程度优于单纯的旋转蒸发或氮气吹干设备。
(3)对需要稳定性和重复性的实验室场景更友好
在生物实验中,“操作的可重复性"往往比"单次最优结果"更重要。JX-ZLN-BN的参数可程序化设定(温度、时间等),设定后仪器自动运行至结束,不需要中途人工判断"差不多了”——这一点对于需要在多批次之间比较数据的实验(如工艺优化、制剂稳定性研究、蛋白组学定量分析)尤为关键。
5. 典型应用场景详解
5.1 酶制剂研究
酶是最典型的活性敏感型蛋白。纯化后的酶液往往浓度偏低,而酶活测定(如Km、kcat的测定)和热稳定性评价都需要一定浓度的样品。浓缩环节如果导致酶活性下降,后续所有动力学数据都将失真。
JX-ZLN-BN的低温运行模式可以在浓缩过程中将温度控制在酶的安全区间内,减少因温度波动造成的活性损失,浓缩后样品可直接进入测定流程。
5.2 抗体与重组蛋白开发
抗体和重组蛋白在纯化后通常需要进行效价测定(ELISA)、亲和力分析(SPR/BLI)、稳定性考察等一系列表征。这些检测对样品浓度和缓冲体系都有明确要求。
真空离心浓缩可以在不引入额外物理接触(如超滤膜吸附)的情况下缩减体积、提升浓度,减少体积、优化缓冲体系,方便后续鉴定与保存。对于需要多个浓度梯度的SPR实验,浓缩后再稀释的操作模式也更加灵活。
5.3 蛋白组学前处理
蛋白组学实验(特别是基于LC-MS/MS的bottom-up蛋白组学)对样品的一致性要求极高。多个样品之间如果因浓缩操作引入的差异过大,会直接影响定量蛋白组学的数据质量。
真空离心浓缩仪的多管并行处理能力和参数一致性,使得批量样品在同一条件下完成浓缩,让样品更适合进入质谱分析流程,提高检测一致性,减少技术变量。
5.4 结构与功能研究
蛋白结晶筛选通常需要较高浓度的蛋白溶液,且蛋白必须保持良好的单分散性,不能有聚集体。冷冻电镜(Cryo-EM)制样同样对蛋白浓度和均一性有严格要求。
相比加热蒸发等粗暴手段,低温真空离心浓缩在提升蛋白浓度的同时,尽量避免了因局部过热而导致的非特异性聚集,为结晶、电镜或相互作用分析提供更稳定的样品状态。
6. 总结
蛋白质纯化后处理是整个蛋白制备流程中不可忽视的关键环节。在"浓缩"这个看似简单的操作背后,蕴含着对样品活性保护、缓冲体系兼容性、操作重复性的多重考量。
真空离心浓缩技术通过离心-真空-控温三重联合机制,提供了一种在低温条件下高效去除溶剂的技术路径,尤其适合温度敏感型蛋白、多批次并行处理以及对批次一致性要求较高的实验场景。
净信JX-ZLN-BN真空离心浓缩仪(升级冷冻款)凭借-10℃至100℃的宽幅控温能力和三重联合工作模式,为蛋白、酶类及胞内活性物质等样品的纯化后处理提供了一个兼顾效率与保护的技术方案。对于蛋白样品来说,很多时候不是"能不能浓缩",而是"浓缩后活性还在不在"——这正是低温真空离心方案的价值所在。






